国际山地医学学会将海拔高度分为高海拔(1500~3500m)、超高海拔(3500~5500m)、极高海拔(>5500m)。我国高原地域广袤,约 26.8% 的国土处于高海拔,包括西藏自治区全境、青海省大部,以及四川、云南、甘肃和新疆的部分地区。每年约1亿人次因工作、旅游或居住进入高原。因特殊地理与气候,高原人群心肺功能及相关疾病的发生、发展和表现独特。初入高原人群急性高原病发生率达36.7%~57.5%,进入海拔越高、上升越快,发生风险越高。外来人员移居不同海拔高原地区,慢性高原病患病率为2.1%~37.4%。长期(≥1年)居住高原人群更易患心肺疾病,高血压、慢性心力衰竭、肺动脉高压患病率分别为31.4%、4.84%、6.2%。因此,准确评估高原人群心肺功能,对疾病诊断与鉴别、预后评估、干预效果评价、运动处方制订等十分必要。
心肺运动试验(cardiopulmonary exercise testing,CPET)作为评估心肺储备能力的金标准,在高原地区具有重要应用价值。但因高原环境的特殊性,高原CPET的广泛开展仍面临诸多挑战。一是高原的低氧、低压、低温、高辐射环境,导致CPET操作安全性降低,因此需要更加严格地把握适应证和禁忌证。二是特殊环境下,需要有更严格的设备质控方案,同时必须提高医护人员的急救能力并设置完整的应急预案。三是缺乏统一的高原数据参考范围,需要结合高原的生理特点设置不同的参考范围和参数解读方案。为规范高原地区CPET的临床应用,提高诊断准确性与治疗效果,保障医疗质量与安全,本专家组在参考国内外相关专家共识、指南及研究成果的基础上,结合高原地区实际情况与临床经验制定了本共识。本共识旨在为高原地区临床医师及相关专业人员提供CPET应用的指导与建议,促进CPET在高原地区的合理、规范开展。
1 高原环境下的病理生理学变化
1.1 高原心血管系统的病理生理变化
在高原低氧环境下,心血管系统会通过一系列复杂的生理机制进行适应性调节。心脏的适应性改变与进入的海拔高度和高原停留时间密切相关。急性高原低氧暴露时(初抵高原),外周化学感受器感知低氧后,激活交感神经并抑制迷走神经张力,导致静息心率显著增快,由心率增快驱动心排血量明显增加。低氧诱导的肺血管收缩和肺动脉压升高可导致右心室后负荷明显增加,健康个体通常能通过增强收缩力等机制代偿,维持右心室功能,但在高强度运动或极端海拔下,可能出现右心室收缩功能下降及不同步性增加。急性暴露时,每搏量的轻微下降可能与右心室压力升高对室间隔的机械作用和心率增快导致心室舒张充盈期时间的缩短有关。左心室收缩功能增强或维持,表现为左心室射血分数、平均标准化收缩期射血率、收缩压/收缩末期容积峰值、左心室扭转、左心室收缩应变率、左心室解旋等指标不变或改善。左心室舒张功能则可能出现轻度减退,表现为舒张早期与晚期充盈速度比值、舒张早期心肌运动速度降低。急性高原暴露时,血压的变化受到交感神经与局部因缺氧产生和释放的扩血管代谢物的双重影响,24h的动态血压变化表现为收缩压和舒张压均显著增高,其中以晨峰血压、夜间血压和舒张压增加为主,勺型血压个体表现出更好的高原心脏代偿和低压适应能力。
随着持续缺氧,机体启动慢性代偿机制如红细胞增多、毛细血管密度增加,心血管系统过度活跃状态逐渐缓解,静息心率逐渐减慢,但仍接近或高于平原水平。由于血浆容量减少及低氧性肺动脉高压导致的右心室后负荷增加等原因,每搏量略降低。慢性低氧持续刺激肺血管收缩,进而导致肺血管重构,造成肺动脉压长期升高。为克服持续升高的后负荷,右心室通过心肌细胞肥大、间质纤维化等途径启动代偿性重构,最终发展为以右心室肥厚、右心室腔扩大为特征的不可逆性结构改变,并可能伴有收缩和(或)舒张功能异常。左心室可出现向心性重构,收缩功能增强或保持正常,但常伴随舒张功能持续减退。
1.2 高原呼吸系统的病理生理变化
在高原低氧环境下,呼吸系统也会发生一系列从急性代偿到慢性适应的精准调控,包括增强通气、优化气体交换和改变肺循环等方面,其目标是最大化肺泡氧分压和动脉血氧饱和度(arterial oxygen saturation,SaO2)。急性期反应(数分钟至数周)为通气驱动增强,颈动脉体化学感受器感知到动脉血氧分压(arterial partial pressure ofoxygen,PaO2)下降后,强烈兴奋延髓呼吸中枢,导致潮气量和呼吸频率增加,使得静息和运动状态下的分钟通气量均显著高于平原水平,可有效提升肺泡氧分压,是积极的代偿机制;然而其副作用是导致低碳酸血症和呼吸性碱中毒。碱中毒会增加血红蛋白对氧的亲和力(左移氧解离曲线),不利于组织释氧,同时也会反馈性抑制呼吸中枢,与低氧的刺激作用形成拮抗,从而限制急性期通气反应的充分性。此外,低氧性肺血管收缩是重要的局部调节机制,旨在减少低通气区域的血流,优化通气-灌注匹配。
长期低氧诱导低氧性肺动脉高压,这不仅是肺血管持续性收缩的结果,更是血管壁结构重构(包括肺动脉中层平滑肌肥厚、内膜增生和非肌性血管肌化)的后果。持续的肺动脉高压是高原肺水肿的病理基础和发展为高原心脏病的核心环节。其他长期适应性改变尚包括胸肺顺应性降低和呼吸肌功能适应性增强等。肾脏代偿与“碳酸氢根洗脱”是慢性适应的核心环节。持续过度通气导致的呼吸性碱中毒,通过2~3d的延迟后,引发肾脏代偿性排出碳酸氢根,血液和脑脊液pH逐渐恢复正常。
2 高原CPET的适应证和禁忌证
MAFLD定义为遗传易感个体由于营养过剩和胰岛素抵抗引起的慢性代谢应激性肝病,主要本共识在CPET平原常规用途基础上,增加了一些针对高原环境的适应证。禁忌证需要在参照平原应用规范的同时,进行更严格的筛选。儿童、孕妇不建议在高原进行CPET。
2.1 CPET的适应证
2.1.1 初入高原或进入更高海拔地域移居者疾病风险评估
评估其对高原低氧环境心肺适应能力,排查潜在心肺功能异常,指导健康管理,预测急性高原病。重点关注有高原反应病史且1d内上升>2800m、1d内登上3500m以上海拔、快速登山、有高原脑水肿或肺水肿病史的人员。
2.1.2 世居高原地区者疾病风险评估
筛查隐匿性心肺功能问题,评估慢性高原病严重程度,揭示静息下不易察觉的病理改变,评估高原慢性病对心肺运动能力的影响。
2.1.3 各种高原疾病的诊治及评估
(1) 高原缺血性心脏病:对疑似心肌缺血患者进行诊断分层,敏感性和特异性高于运动负荷下心电图。
(2) 慢性心力衰竭:是评估运动耐量的“金标准”。
(3) 肥厚型心肌病:区分生理性和病理性左心室肥厚,预测发病及分层。
(4) 心脏瓣膜病:评估严重程度、预后和术后效果。
(5) 肺动脉高压和慢性阻塞性肺病:无创识别通气 - 灌注异常,为筛查和预后评估提供参考。
(6) 间质性肺病:为筛查和预后评估提供依据,评估劳力性呼吸困难和运动不耐受,有助于制定康复计划。
(7) 诊疗效果监测:术前风险评估,监测干预效果,为诊疗策略调整提供依据。
2.1.4 特殊人群的健康评估与运动指导
(1) 对高原地区工作者(军人、航天人员、矿工等)入职前评估心肺功能达标情况、作业期间监测健康及职业风险分层,降低不良事件风险。
(2)对专业运动员、登山爱好者等,制定训练方案、监控效果、评估运动能力极限,预防运动相关高原病,量化高原习服效率,预测适应程度。
2.2 CPET的禁忌证
2.2.1 绝对禁忌证
急性冠状动脉综合征、急性心力衰竭、有症状的重度主动脉瓣狭窄等;急性主动脉夹层、急性心肌炎等;重度肺动脉高压、严重心律失常等;急性肺栓塞及肺梗死、急性呼吸衰竭等;未控制的哮喘、外周血氧饱和度<85%等;急性下肢深静脉血栓;近期非心脏原因影响运动能力或运动加剧病情的疾病;重度高原反应;未获得知情同意。
2.2.2 相对禁忌证
冠状动脉左主干50%以上狭窄或闭塞;无症状的中到重度主动脉瓣狭窄;梗阻性肥厚型心肌病;轻中度肺动脉高压;静息心率>120次/min;未控制的高血压;近期脑卒中或短暂性脑缺血发作;下肢肌间静脉血栓;未纠正的临床情况;妨碍行走的骨科损伤;精神异常;轻度至中度高原反应;不能配合者。
3 高原CPET的标准化操作流程
3.1CPET检查标准化操作流程
该流程系统分六个核心环节,涵盖从前期准备到长期管理的全过程,保障测试安全与数据准确。
(1) 受试者筛选与环境准备:测试在采光通风好、温湿度适宜的环境中进行,悬挂Borg劳累程度分级表。测试团队由专业人员组成,包括掌握急救措施的心内科、呼吸科或运动医学科医师,负责核心操作的运动康复技师,以及提供护理支持的护师。配备常规急救设备与药物,明确下撤转运预案。
(2) 受试者准备与设备校准:受试者穿舒适运动服饰,餐后2~3h测试,测试前签署知情同意书。对气体流速传感器和分析仪定标校准。
(3) 运动方案选择:高原环境下一般人群推荐踏车运动试验的功率递增方案(Ramp方案),运动员选平板Bruce改良方案。测试前完成静态肺功能测试,并重复测量流速 - 容量环以保障重复性。
(4) CPET 核心操作实施:分四个阶段,静息期(3min)记录基础数据;无负荷热身期(3min)保持踏车速度55~65r/min;功率负荷期(6~10min)密切监测,达终止标准即停;恢复期(6~8min)无负荷慢踏2~3min后停止,观察指标至基线水平。
(5) 运动后评估与留观:测试后通过非诱导式提问了解受限原因。高原运动后心率变异性可能持续降低,建议留观20~60min,防范延迟性风险。
(6) 随访与长期管理:建立分级随访机制,短期(24~72h)电话随访,中期(第6周)用6min步行试验调整运动处方,末期(第12周)重复CPET或6min步行试验,量化功能改善并优化康复计划。此流程通过多阶段闭环管理,兼顾个体化需求与安全保障。
3.2 功率递增幅度按照如下公式计算
预计无负荷摄氧量=150+6×体质量。
预计峰值摄氧量= (身高-年龄)×20(男性)或峰值摄氧量 =(身高-年龄)×14(女性)。
每分钟递增功率=(峰值摄氧量-无负荷摄氧量)/100。
一般建议在6~10min完成递增运动试验。功率递增幅度的选择应在综合考虑受试者的基础生理功能、日常活动能力、心肺功能、高原耐受等状况后决定。对于老年、日常活动量较低、存在严重呼吸或心血管系统疾病的受试者,应酌情减少功率递增幅度;对于运动员或有长期运动习惯者,则可适当提高功率递增幅度。
3.3 终止标准
(1) 出现中度到重度心绞痛。
(2) 出现眩晕、共济失调、发绀、面色苍白、严重疲惫、呼吸困难等症状或体征。
(3) 心电图示相邻导联ST段水平型或下斜型压低≥0.2mV,持续2min及以上;ST段弓背向上型抬高≥0.1mV。
(4) 出现严重心律失常,如二度房室传导阻滞、三度房室传导阻滞、室性心动过速、频发室性期前收缩、新发快速心室率的心房颤动等。
(5) 随着功率递增,收缩压下降≥10mmHg(1mmHg=0.133kPa)或持续低于基线血压;或收缩压≥220mmHg和(或)舒张压≥110mmHg。
(6) 血氧饱和度下降:高原地区外周血氧饱和度低于80%,或较运动前降低幅度超过15%时需立即停止。
(7)因下肢无力或肌肉疼痛、痉挛,导致踏车转速明显下降。
(8)受试者要求终止运动;设备故障:设备异常需终止测试。
3.4 急救设备要求
除常备急救设备和急救车常备药物外,基于高原病还应准备呋塞米、甘露醇、地塞米松、布洛芬、硝苯地平、西地那非、他达拉非等药物。由于存在低血压的风险,应避免联合使用硝苯地平和他达拉非或者西地那非。建议把增加氧气作为优先急救准备。下撤为急性高原病的最优治疗方式,若原地处理无效,应立即下撤至低海拔医疗机构。下撤高度通常为300~1000m,患者不应单独下撤,尤其出现高原脑水肿症状时需专业人员陪同。便携式高压氧舱对于患有严重急性高原病且无法下撤的患者疗效确切;控温毯通过控制体外循环液温来辅助调节体温;抗休克裤通过充气加压促进血液回心。
4 高原CPET的关键参数解读
CPET心血管指标包括:心率、心率储备、心率恢复、血压、氧脉搏、摄氧量功率斜率(∆VO2/∆WR 斜率)等。肺部监测指标根据功能分为三大类:
(1) 反映通气功能的指标,包括呼吸储备、通气量、潮气量、深吸气量、用力肺活量、第1秒用力呼气容积(forced expiratory volume in 1 second,FEV1)、最大自主通气量(maximal voluntary ventilation,MVV)等。
(2) 反映气体交换的指标,包括SaO2、氧通气当量(ventilatory equivalent for oxygen,EqO2,即VE/VO2)、二氧化碳通气当量(carbon dioxide ventilation equivalent,EqCO2,即VE/VCO2)、潮气末氧分压(endtidal oxygen partial pressure,PetO2)、潮气末二氧化碳分压(endtidal carbondi oxide partial pressure,PetCO2)、死腔分数等。
(3)反映代谢的指标,包括峰值摄氧量(peak oxygen uptake,peakVO2)、最大摄氧量(maximal oxygen uptake,VO2max)、无氧阈、二氧化碳排出量(carbon dioxide output,VCO2)、呼吸熵、代谢当量、摄氧效率斜率(oxygen uptake efficiency slope,OUES)等。心肺共同作用的指标包括peakVO2、VO2 max、无氧阈、呼吸交换比(respiratory exchange ratio,RER)、VE/ VO2、VE/VCO2斜率、PetO2/PetCO2、代谢当量以及OUES。
4.1 心率
急性缺氧时静息心率可以代偿性增快10%~15%,初到高原的静息心率常超100次/min。相同运动强度下,高原的静息、运动及运动后恢复心率均显著高于平原。不过,多项研究显示峰值心率会随急性缺氧加剧而下降,海拔8848m处个体最高心率约为海平面的70%。心率储备是最大预测心率与静息心率差值,反映心脏代偿潜能,急性高原暴露后显著降低。心率恢复是运动停止后特定时间内的心率下降值,反映迷走神经张力的快速恢复能力,是心脏自主神经调节功能良好的标志,心率恢复减慢是全因死亡和心血管死亡的独立预测因子。
4.2 血压
血压与海拔高度呈正相关,海拔每升高1000m,血压上升10~20/5~10mmHg。世居高原或移居高原人群静息和运动血压水平均高于平原人群。
4.3 氧脉搏
即摄氧量与心率之比,表示在每次心跳时,身体从血液中摄取并利用的氧气量,反映心血管系统和肌肉利用氧气能力的协同作用。研究发现,急性高原暴露后无氧阈和峰值氧脉搏均显著降低。
4.4 ∆VO2/∆WR
摄氧量随运动强度增加而上升的速率,也被称为有氧做功效率,是评估心功能效率的核心指标之一。在亚极量运动阶段(从无负荷骑行到无氧阈),摄氧量与运动强度通常呈线性关系,斜率的正常值约为10mL/(min·W)。当斜率降低<8.5~9.0 mL/(min·W)时,表明心血管系统无法有效地将氧输送到肌肉,运动效率低下,常见于心力衰竭、肺动脉高压等疾病。临床研究发现,从海拔300m快速到达海拔3900m后,斜率从(9.4±1.0)mL/(min·W)显著降低到(8.2±1.2)mL/(min·W)。
4.5VO2max与peakVO2
VO2max代表极量运动时单位时间内机体摄取和利用氧的最大能力,是评价人体有氧能力的金标准。但并非所有人能达到此平台,临床上常用peakVO2替代。在平原,peakVO2是评估心功能核心指标,其正常值通常为20~50mL/(kg·min),随海拔变化peakVO2变化(表1)。

4.6 无氧阈
是有氧代谢和无氧代谢的临界点,其对应的运动强度或摄氧量水平是评价个体有氧耐力和心肺功能的黄金指标。无氧阈不受主观努力程度的影响,比VO2max更能反映日常活动的有氧能力。高原暴露时,机体更早启动无氧代谢代偿,无氧阈明显降低,较低运动强度下就会出现乳酸堆积,且返回平原后并不能立即恢复。
4.7 呼吸熵与RER
呼吸熵是细胞代谢水平的理论值,而RER是肺部气体交换测量的实际值。RER=VCO2/摄氧量,表示运动时的瞬时气体交换比值,常用于判断运动强度是否达到极限。在高原由于氧供不足,机体更早依赖糖代谢供能,导致亚极量运动时的RER较平原升高。但长期习服后,随着代谢效率改善,RER可逐渐回落至接近平原水平。
4.8 VE/VO2与VE/VCO2 VE/VO2
升高提示氧摄取效率降低,VE/VCO2升高则提示CO2排出效率下降。急性高原暴露时,VE/VO2和VE/VCO2均显著升高,这与低氧导致通气增加而摄氧量、VCO2相对降低有关,提示通气-灌注失衡。在3000m海拔,亚极量运动时VE/VCO2可从平原的25增加至30以上。
4.9 PetO2与PetCO2
正常时PetO2和PetCO2静息值接近动脉血值。两个指标主要受通气-灌注影响,在高原环境会随大气氧分压等因素改变。运动初期,PetCO2明显上升(可达42~48mmHg),中等强度运动时保持平台期,无氧阈后过度通气排出大量CO2,使PetCO2缓慢下降。PetO2静息值略低于吸入气氧分压,运动中轻度上升,无氧阈后显著上升。
4.10 代谢当量
1代谢当量按每千克体质量每分钟摄氧3.5mL定义。高原总体低于同龄平原人群,表现为心排血量储备下降,肺泡换气受限,骨骼肌有氧代谢效率降低,氧输送/利用受限。目前,高原地区测试代谢当量的研究有限,参照平原标准,代谢当量<5mL/(kg·min)时为预后不良。
4.11 OUES
OUES描述了在整个运动过程中摄氧量相对于通气量的对数变化关系。OUES值越高,表明机体能够以更少的通气量摄取更多的氧气,用于综合评价心肺系统的整体功能效率,是CPET中一项重要的亚极量运动指标。在心力衰竭、肺动脉高压等患者中,OUES值通常显著降低。在高原,急性低氧暴露会降低OUES,而高原适应者则能维持甚至优化OUES。
4.12 最大运动通气当量(maximal ventilatory equivalent,VEmax)与呼吸储备
VEmax是指运动时所能达到的最大通气量,而呼吸储备为MVV与VEmax的差值(或百分比)。急性高原暴露时静息及运动时的通气量显著增加,VEmax可较平原升高10%~30%;呼吸储备相应降低。研究显示,在高海拔(>4000m)运动时,呼吸储备可降至10%以下(远低于平原的20%~30%)。
4.13 潮气量与深吸气量
潮气量指平静呼吸或运动时每次吸入或呼出的气体量;深吸气量指平静呼气末用力深吸气能吸入的最大气体量,代表“肺储备容积”。运动强度增加,潮气量会逐渐占用深吸气量;若运动中深吸气量显著降低、潮气量接近或达到深吸气量水平,提示动态肺过度充气。在高原,机体通过增加潮气量应对低氧,导致呼吸储备下降,高原适应者或通过优化肺容积和通气控制减轻不利影响。
4.14SaO2
高海拔运动负荷下的SaO2显著低于同海拔静息状态及低海拔相同运动负荷的水平,运动前后SaO2的下降值与海拔和运动负荷呈正相关。
4.15VCO2与最大VCO2
VCO2与通气效率相关。高原运动时,无氧代谢提前启动,糖酵解产生的乳酸缓冲后释放更多CO2,使亚极量运动时VCO2较平原升高。同时,低氧性通气增加,加速CO2排出,降低动脉血二氧化碳分压。最大 VCO2在高原随海拔升高而下降,与VO2 max类似,反映整体代谢率降低。
4.16 肺一氧化碳弥散量 (diffusing capacity of the lung for carbon monoxide,DLCO)
DLCO是通过单次呼吸法测定气体经肺泡-毛细血管膜扩散能力的核心指标。其原理基于一氧化碳与血红蛋白的高亲和力特性,正常参考值为26.5~32.9mmHg。2022版GOLD指南强调了DLCO在慢阻肺评估中的重要性,研究指出,DLCO值低于60%预测值的患者全因死亡率显著升高。
5 CPET参数的临床应用
5.1CPET 九宫图
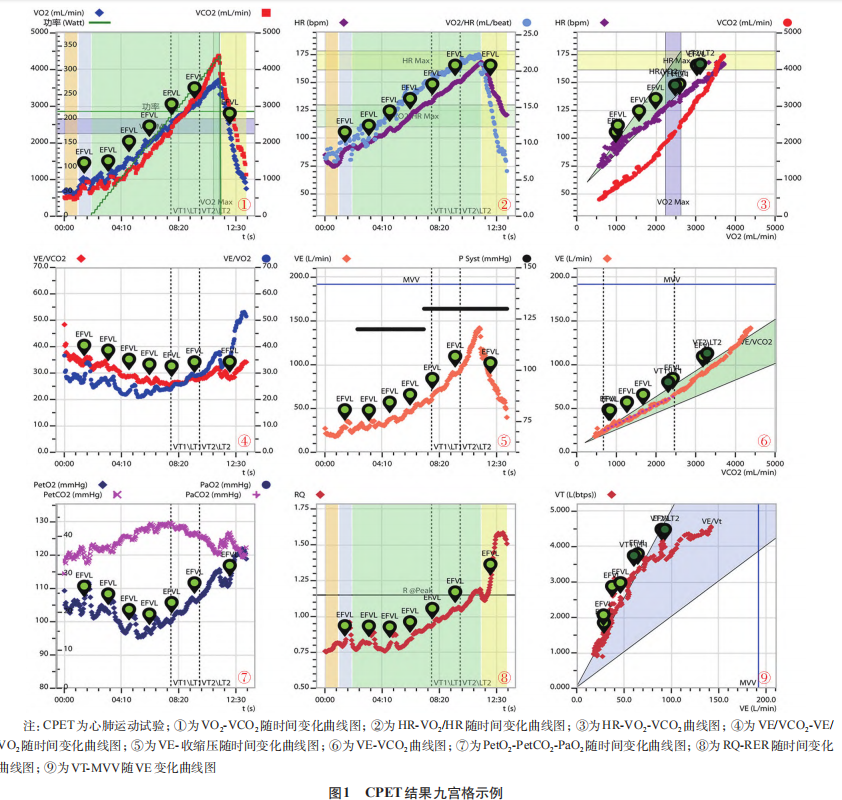
CPET 的参数解读常用九宫图表示(图1):
(1) 摄氧量-VCO2随时间变化曲线:反映二者动态关系,正常时线性增长,心力衰竭或肺血管疾病患者,VCO2亚极量运动时可能相对升高,提示无氧代谢提前启动。
(2) 心率-氧脉搏随时间变化曲线:反映心率及氧脉搏随运动负荷的变化,慢性心力衰竭和缺血性心脏病患者,心率反应可能异常,氧脉搏曲线低平或峰值降低,提示心血管储备功能下降。
(3) 心率 - 摄氧量 -VCO2曲线:综合反映三者交互变化,高原或心肺疾病时,摄氧量增长迟缓,提示心肺功能整合能力受损。
(4) VE/VCO2-VE/VO2随时间变化曲线:是评估通气效率的关键,肺血管疾病和心力衰竭患者,VE/VCO2斜率显著升高、最低值消失,反映通气 - 灌注失调和生理死腔增大。
(5) 通气量 - 收缩压随时间变化曲线:反映二者在运动中的关系,心力衰竭或严重缺血性心脏病患者,收缩压反应减弱,可能出现运动性低血压,通气量代偿性增加,提示心排血量不足和循环功能受限。
(6) 通气量-VCO2曲线:反映二者关系,高原适应不良或肺部疾病时,曲线左移,VE/VCO2比值升高,提示气体交换效率下降和呼吸代偿增强。
(7) PetO2-PetCO2-PaO2随时间变化曲线:反映三者动态变化,间质性肺疾病或肺血管病患者,PetO2和PetCO2曲线低平或下降,PaO2明显降低,反映肺泡-毛细血管膜弥散功能障碍和气体交换异常。
(8) 呼吸熵-RER随时间变化曲线:反映运动时能量代谢底物变化,高原低氧环境下,亚极量运动时呼吸熵、RER值升高,长期习服后可能回落。
(9) 潮气量-MVV随通气量变化曲线:描述潮气量与用力肺活量随分钟通气量的变化,COPD患者潮气量响应早期出现平台期,潮气量/深吸气量比值接近或超过0.8,MVV明显降低,呼吸储备常低于20%。
5.2CPET在高原心肺疾病诊断与疗效评估中的应用
(1) 心力衰竭:主要特征为心脏泵血功能下降导致的运动耐量受损,心力衰竭患者peakVO2显著下降,无氧阈提前出现;氧脉搏、∆VO2/∆WR降低;收缩压偏低,严重者可出现运动性低血压及特征性震荡呼吸。同时存在轻度通气-灌注比例失调和气体交换效率低下:VE/VCO2斜率通常为34~45,OUES降低,PetCO2在运动中微弱增长(表2)。图1九宫格图中的①②④⑤⑥有相应指标改变,可概括为“低心排量伴高通气-灌注失衡”。CPET也是量化治疗反应的关键工具。沙库巴曲缬沙坦能提高射血分数降低的心力衰竭患者的peakVO2及氧脉搏,降低VE/VCO2斜率(对心功能和通气效率的改善);HF-ACTION研究表明,运动康复提高peakVO2约0.5mL/(kg·min),降低了射血分数减低的心力衰竭患者7%的全因死亡和住院联合终点风险。
(2) 缺血性心脏病:主要表现为心肌缺血诱发左心室功能障碍,极量运动能力受损。核心特征是peak VO2下降,常无法达无氧阈,是冠心病严重程度独立危险因素;∆VO2/∆WR曲线有“拐点”(心肌缺血阈值);氧脉搏低平且峰值降低(心肌缺血致每搏输出量受限);PetCO2轻度增长;有运动性低血压(表2)。研究显示,急性心肌梗死患者12个月后在高原的运动最大功率、peakVO2及运动持续时间显著降低,分别约15%、19%和16%。图1九宫格图中①②⑤指标改变明显,可概括为“缺血阈值诱导的功能骤降”即拐点。此外,CPET可评估血运重建、药物及康复训练综合疗效:缺血性心肌病患者经曲美他嗪联合运动训练干预8周后peakVO2可提高25%;心肌梗死患者急诊介入治疗后,急性期内达到无氧阈时摄氧量≥10.5 mL/(kg·min)提示未来2年预后更佳。
(3) 肺血管疾病:主要特征为通气 - 灌注严重失衡与气体交换障碍。研究显示,在海拔2500m情况下,肺血管疾病患者最大运动功率下降约11%,恒定负荷运动时间缩短 22.9%。表现为通气效率的极度异常:VE/VCO2斜率显著升高左移(>45);运动中PetCO2早期即下降;进行性运动性低氧血症(SaO2下降);极低且呈平台样的氧脉搏(右心室射血严重受限)。图1九宫格图中的①④⑥⑦有相应指标改变,可概括为“通气-灌注解离伴气体交换障碍”。有研究证实,肺血管疾病治疗后peakVO2的改善与病死率降低相关。
(4) 先天性心脏病:表现具有高度异质性,同时具有心脏储备功能耗竭与独特的通气血流比例失调。特征表现为无氧阈提前出现,峰值心率无法达到预期最大值;收缩压反应不良(上升不足、平台或下降)是高风险标志;部分类型(如存在右向左分流)可出现特征性的运动性SaO2下降;呼吸储备可能增高,反映通气受限非主要因素。Fontan术后患者中VE/VCO2值的显著升高表明其气体交换效率受损的风险较高。中、重度先天性心脏病患者前往海拔1800m以上地区前应接受全面评估;病情稳定、无贫血的简单先天性患者可考虑高海拔旅行,但需充分告知相关风险。
(5) 慢性阻塞性肺疾病:其主要特征表现为呼吸储备显著降低(储备降低);潮气量响应曲线早期出现平台期(动态过度充气);peakVO2和氧脉搏下降;通气当量、VE/VCO2斜率升高,PetO2及PetCO2变化减小(存在显著增大的通气-灌注失调与生理死腔);∆VO2/∆WR降低(氧输送到肌肉受限,表2)。图1九宫格中的②③④⑥⑦⑨可能出现相应改变,可概括为“通气限制”模式,伴有“气体交换效率低下”和“心血管系统受累”
(6) 间质性肺疾病:主要病理基础为肺间质的炎症与纤维化导致弥散膜增厚及肺泡毛细血管床毁损,其最具特征的表现包括:VE/VCO2斜率显著增高,且最低值消失或异常升高;PetO2与PetCO2曲线低平或进行性下降;氧脉搏低平及峰值降低(右心后负荷增加及心排血量受限);并呈现高频率、低潮气量的浅快呼吸模式(表2)。图1中的②③④⑥⑦可能出现相应改变,其在九宫格图中的表现为以气体交换严重障碍为主导的典型模式。
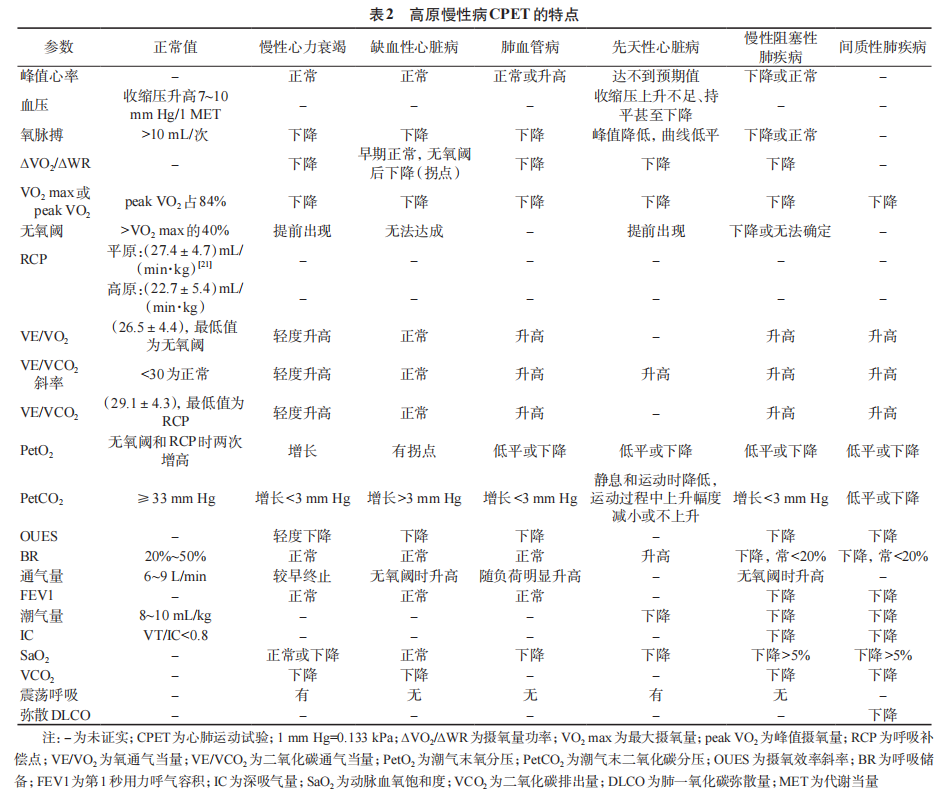
(7) 高原慢性支气管炎与支气管扩张症:其主要特征表现为混合型通气异常模式。潮气量响应曲线的平台期提前及呼吸频率代偿性增快;peakVO2常呈不成比例的降低;VE/VCO2斜率轻至中度增高(通气-灌注失调与生理死腔增加)。在九宫格图中的②③④⑥可能出现相应改变。
CPET为高原慢性心血管和呼吸系统疾病的精准医疗提供了强大的技术支撑。它从整体生理学角度揭示了疾病的复杂面貌,是实现从“静息病理”到“运动功能”评估范式转变的关键,其解读及临床应用应遵循“模式识别”原则,综合判断功能受限的主导机制(通气、循环、气体交换、外周),而非孤立看待单个参数。
5.3CPET在运动员高原训练中的应用
在运动医学领域中,CPET广泛用于运动员训练监测和评估,VO2max是重要指标。多数研究表明,平原VO2max较高者高原暴露时下降幅度更大,优秀运动员在海拔580m处就可能出现 VO2max下降。对39例攀登珠峰受试者的研究显示,6022m海拔时 VO2max下降(40.5±13.7)%,习服后该指标显著改善。通过心肺功能测试可识别可能无法登顶的登山者,计划不使用辅助供氧登山时,基线 VO2max 低于49.0mL/(kg·min)的攀登者登顶失败概率达83.3%;初次攀升至 4844m 后血氧饱和度下降超14%,可能面临急性高山病 。此外,低压低氧暴露结合登山训练时,中等海拔世居女性标准运动时能维持更高的SaO2。10名登山者连续30d滞留海拔4900m后,无氧阈从平原的(39.3±8.0)mL/(kg·min)降至(27.8±5.6)mL/(kg·min)。对41例珠峰攀登者的调查显示,超1/3攀登者攀登期间出现心律失常。
因此,拟进入高原训练的运动员需在平原完成一次标准化CPET测试,获取VO2max、无氧阈、VE/VCO2斜率等关键参数作为生理基线,这些数据是评估高原适应与训练反应的重要参照。基于CPET指标对运动员进行危险分层,确立运动强度、时长与频率,制订科学个体化运动处方。高原训练期间,每周至少进行1次CPET测试,配合每日SaO2和心率变异性监测。高原训练急性期(1~3d)以低强度有氧训练为主,适应期(4~14d)逐步增加强度,稳定期(>14d)可谨慎引入高强度间歇训练,期间密切观察CPET参数动态变化。若peakVO2下降超10%,或SaO2持续低于85%,考虑进行适应性训练,如渐进式上升海拔并停留适应,或在医生指导下用药,同时及时调整训练计划,如降低强度、增加恢复时间或安排低海拔适应性调整,防范过度训练和运动性缺氧。
5.4CPET在高原作业人员中的应用
海拔升高至2000~4000m时,高原作业人员(军人、登山者、矿工等)心率、单位体表面积能量代谢率明显下降。一般将最大代谢当量<5MET作为残疾标准,建议职业(8h/d)平均能量消耗水平不超患者峰值代谢当量的40%,峰值强度不超80%。近年国内一项前瞻性临床试验[年龄(36.5±6.5)岁,女性占35.9%显示,从海拔300m急进到3900m后,VO2max、无氧阈、呼吸补偿点摄氧量、VO2/WR 斜率、代谢当量、峰值RER、无氧阈 RER均显著降低。国外试验表明,极量运动时平原与海拔3800m最大运动心率无显著差异,但MVV和SaO2差异明显 。对不同海拔青年人运动能力研究发现,<500m、3850m、4550m海拔下,VO2max和SaO2依次降低,提示其在评价高原有氧能力时很重要。CPET中的SaO2和心率变化量可早期识别急性高原病高风险人群,低中强度有氧训练更适合提升高原移居者心肺功能。
6 未来研究方向
尽管 CPET 在高原训练监控中的应用正逐步获得认可,当前研究仍存在诸多值得完善之处,未来的探索可在以下方向持续深化。
(1) 构建高原特异性的CPET参考区间与解释框架:现有CPET参考值多基于平原人群建立,直接应用于高原环境存在局限。未来应通过多中心、多海拔梯度的大样本研究,构建高原CPET数据共享平台,建立适用于高原人群的分层参考区间,并结合峰值指标(如peakVO2)及次极量运动参数(如VE/VCO2斜率、氧脉搏等)进行动态解读,以提升评估的准确性和可比性。
(2) 多模态生理监测与CPET的整合应用:单一CPET难以全面反映高原训练中的复杂生理负荷。便携式近红外光谱、连续脉搏血氧监测和心率变异性分析等技术,已在运动阈值识别和急性高原病预测中展现出潜力。将这些无创监测手段与CPET 结合,可构建更为系统的高原训练动态监控体系。
(3) 人工智能与机器学习支持的个体化监控:基于CPET、血氧、心率变异性分析及训练负荷等多源数据的人工智能方法,已初步用于高原病的风险预测。未来着力开发可解释性强、泛化能力好的算法模型,不仅可以实现并发症的早期预警,还可辅助估算peakVO2与无氧阈,为制订完全个性化的训练方案提供依据。
(4) 开展训练模式优化与“回平原窗口期”循证研究:“高住低练”模式可提升竞技表现,但最优高度等参数有待明确,且回平原参赛最佳时间有个体差异,需用CPET纵向监测判定。
(5) 进行不同运动项目与特殊人群差异化研究:不同项目运动员对高原暴露生理反应有差异,特殊人群高原适应性训练安全阈值确定需进行针对性CPET研究。总之,CPET正从传统评估工具向综合平台发展,通过构建标准、整合监测、引入新方法及加强随访,未来其在高原应用的价值与效能将显著提升
7 总结
CPET作为一种在运动状态下评估心肺储备功能和运动耐力的医学检查方法,不仅在高原环境下评估人体心肺功能、运动耐量与生理应激反应中发挥关键作用,而且在高原适应能力评价、作业能力评估、疾病筛查、风险预警及科学运动指导方面具有不可替代的临床价值。该测试可客观反映低氧环境下个体的有氧能力、功能储备与代偿机制,尤其适用于高原世居人群、短时驻留人员、登山者、运动员以及心脑血管疾病高危人群的健康管理与个体化运动处方制定。
参考文献:略
作者:略
单位:老年疾病国家临床医学研究中心(解放军总医院)
中国老年保健医学研究会老年心血管病分会
中国老年学和老年医学学会呼吸与危重症医学分会
北京医学奖励基金会
来源:中华老年心脑血管病杂志2026年1月第28卷第1期
声明:
1.本网站所有内容,凡是注明 “来源:心脏康复网”的文字、图片和音视频资料,授权转载时须请注明“来源:心脏康复网”。
2.本网所有转载文章系出于学术分享的目的,版权归原作者所有。如有侵权,请及时联系我们更改或删除。